En el post anterior vimos los modelos atómicos de algunos de los científicos los cuales utilizaríamos en este tema, por lo cual si aún no haz visto mi post anterior te lo recomiendo.
En los átomos los electrones no están distribuidos al azar, se acomodan en subniveles y orbitales de tal modo que su organización sea lo más estable, esto tiene nombre como «configuración electrónica».
Los electrones llegan a los orbitales y los subniveles de una forma ordenada ya que se inicia en los subniveles internos y continua hacia los extremos.
Los electrones saturan en primer lugar «s» «p» y así sucesivamente.
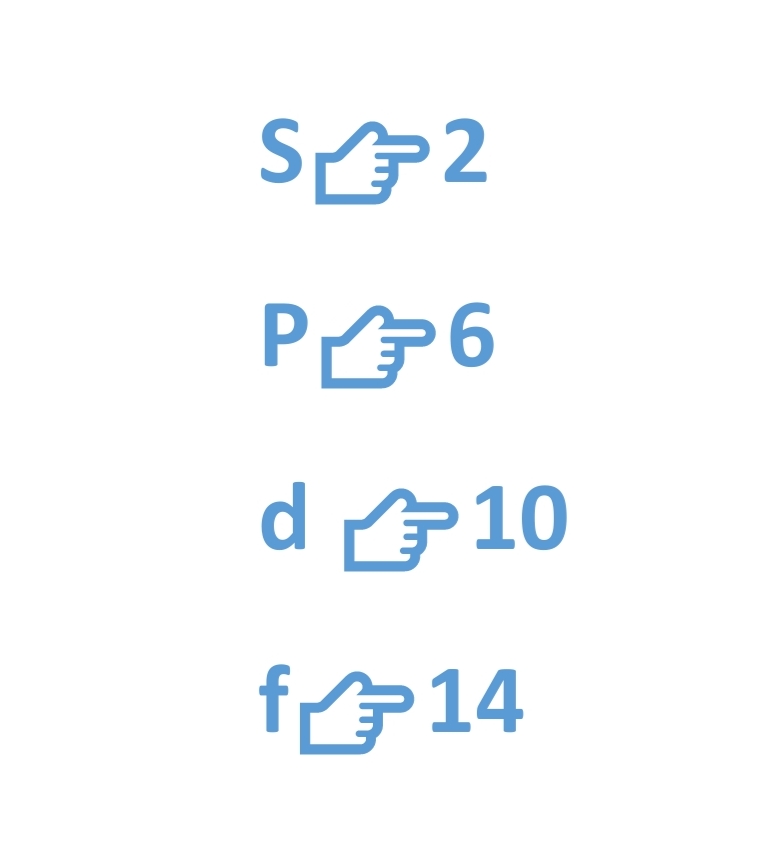
Los electrones se ordenan en determinados sitios del espacio atómico denominados orbitales, hay 4 tipos los cuales alcanzan un número máximo de electrones con orbital es decir:
Para desarrollar la configuración electrónica es necesario utilizar la «Tabla de las Diagonales» la cual se forma de la siguiente manera:

⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐
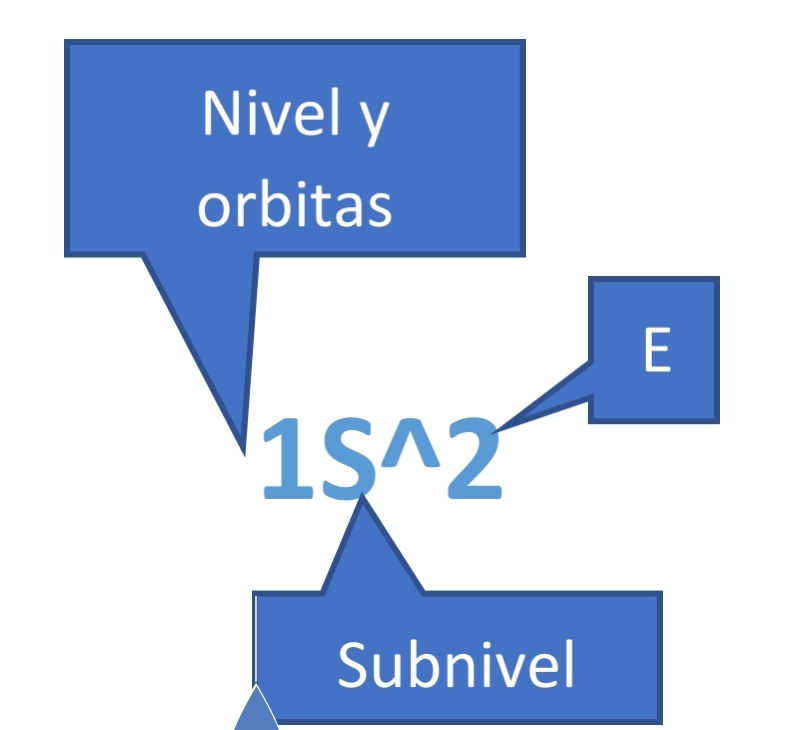
Ahora sí, esto es utilizado de esta manera y también se utiliza el modelo de Bohr visto en el post anterior, este es un ejemplo de como se desarrolla la configuración electrónica de los elementos:
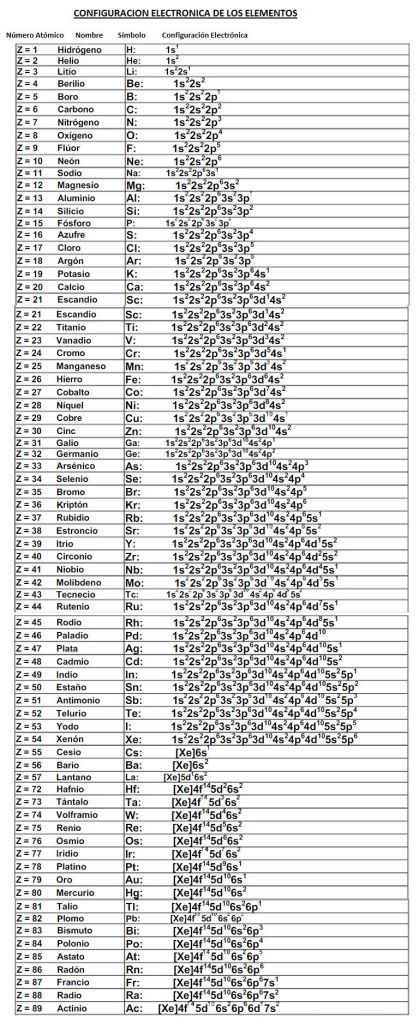
Este sería el ejemplo de como se desarrolla la configuración electrónica, como puedes ver tan solo se va siguiendo la tabla de las Diagonales hasta llegar a el número atómico el cual es el elemento.
Cómo el hidrógeno tiene como número atómico el 1 tan solo se utiliza el 1S^1 para poder llenar este elemento, pero cuando es un elemento con un gran número atómico este requiere de más presicion para poder llegar hasta su número átomico
Y así es como concluiriamos la clase de hoy espero te haya funcionado y cualquier duda háganmela llegar.
-señorita umbrella-
