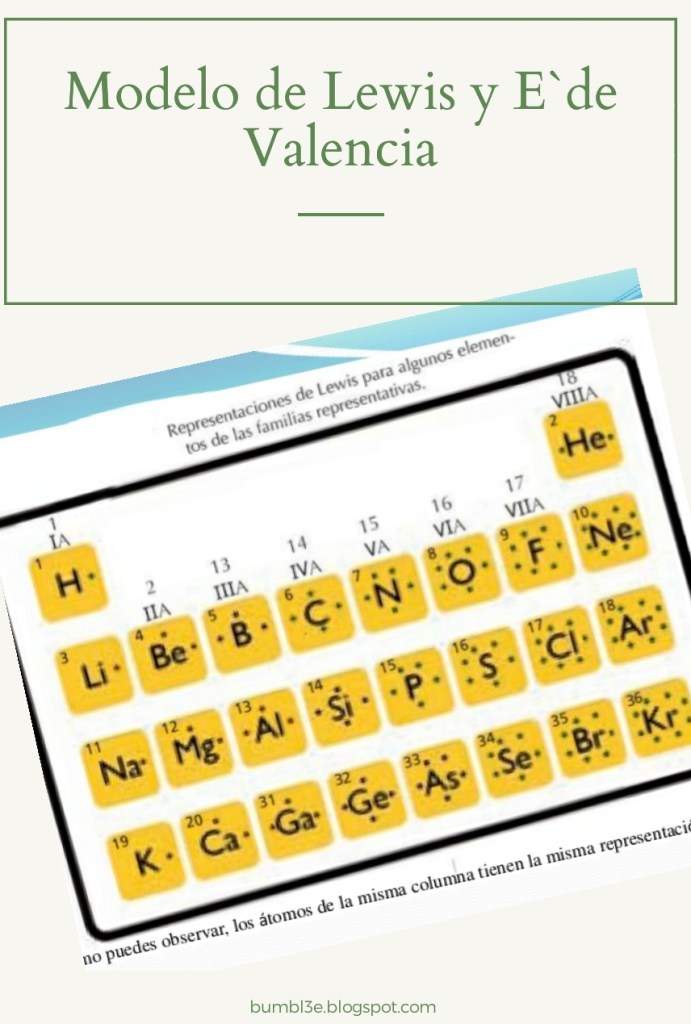
En 1916 el químico estadounidense Gilbert Newton Lewis (1875-1946), formuló un modelo para presentar los enlaces químicos entre los átomos, el cual explica por qué algunos elementos se unían con otros y los compuestos así formados tenían estructuras determinadas.
La regla del octeto o teoría del octeto que les propuso indica:
que la tendencia de los átomos de los elementos químicos es completar sus últimos niveles de energía con una cantidad de electrones tal que adquiere una configuración semejante a la de un gas noble,es decir los átomos tienden a ser estables cuando tienen ocho electrones en su capa de Valencia
Enlace Quimico.- fuerza de atracción electrostática que mantiene unidos a los átomos en compuestos o moléculas.
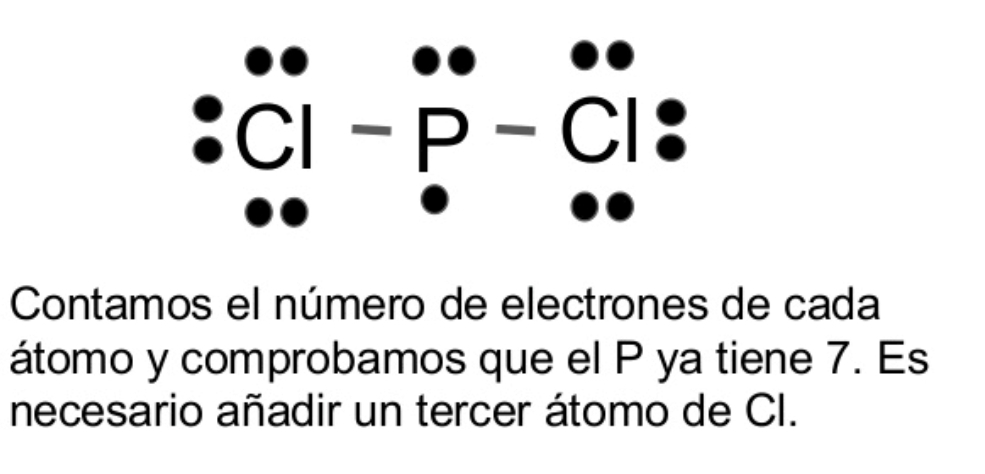
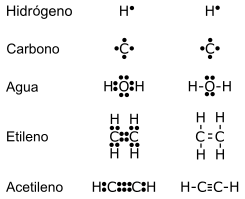
El modelo de Lewis consiste en escribir «El símbolo del elemento químico y a su alrededor un número de puntos o cruzes = que el número de electrones de Valencia, ejemplos»
⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐⭐
¿COMO SE ENLAZAN LOS ELECTRONES PARA FORMAR MOLÉCULAS?
🔴 los químicos en sus investigaciones han observado que los gases nobles o inertes como son (He,Ne , Ar, Le, Xe) son químicamente estables puede suponerse que su estabilidad se debe a que tienen ocho electrones en su último nivel de energía la mayoría de los elementos químicos no se encuentran libres en la naturaleza forman parte de diversas sustancias.
Por lo tanto para formar moléculas o compuestos los átomos pierden aceptan o comparten electrones, lo cual también lo utilizaremos en siguientes clases.
para combinar un elemento con otro se necesita primero dar paso a la tabla de diagonales y luego colocar los puntos o cruzes correspondientes algo así: